分子的形状是三角锥形尿素易溶于水,主要原因是尿素分子和水分子之间能形成氢键.
(2)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,NH3分子中氮是sp3杂化,氮周围有一对孤对电子对;尿素分子和水分子之间能形成氢键,所以尿素易溶于米乐M6 米乐平台水;
(2)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素,所以C、N、O三种元素的第一电离能由大到小的顺序为:N>O>C;NH3分子中氮是sp3杂化,氮周围有一对孤对电子对,所以NH3分子的形状是三角米乐 登录入口锥形;尿素分子和水分子之间能形成氢键,所以尿素易溶于水,故答案为:N>O>C;三角锥形;尿素分子和水分子之间能米乐M6 米乐平台形成氢键;
(3)原子个数相等价电子数相等的微粒是等电子体,碳酸根与硝酸根离子互为等电子体,故答案为:CO32-;
(4)晶胞示意图中铁和氧的原子个数都是4,所以氧化物的化学式为:FeO,故答案为:FeO.
点评本题是对物质结构的考查,主要考查均摊法及晶胞结构的计算等基础知识,正确判断晶体结构是解题的关键,注意立体几何知识在解题中的灵活运用,难度中等.
(3)与CO2互为等电子体的一种阴离子为SCN-(填化学式);常温下CO2呈气态,而H2O呈液态,其主要原因为水分子之间存在氢键.
(4)将KMnO4在空气中焙烧可制得Mn3O4,Mn3O4中Mn元素的化合价为:+2和+3.
(1)磷元素原子核外最外层电子排布式为3S23P3.NaH2PO2中涉及到四种元素,它们的原子半径由小到大的顺序为H<O<P<Na(填元素符号).
(3)海产品添加剂多聚磷酸钠是由Na+与多聚磷酸根离子组成的,某种多聚磷酸根的结构如图.
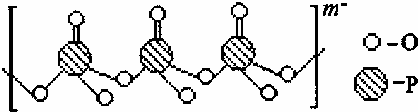
①原子的杂化类型为sp3.②这种多聚磷酸钠的化学式为Nan+2PnO3n+1.
①NaH2PO2为正盐(填“正盐”或“酸式盐”),其溶液显弱碱性(填“弱酸性”“中性”或“弱碱性”)
②次磷酸钠(NaH2PO2)可用于化学镀镍.化学镀镍的溶液中含有Ni2+和H2PO2-,在一定条件下能发生如下反应生成Ni和H2PO3-,写出上述反应离子方程式H2O+Ni2++H2PO2-═Ni+H2P米乐 登录入口O3-+2H+.

