我国硒含量居世界首位,硒广泛用于冶金、陶瓷、电子、太阳能等领域。工业上常将含硒废料处理得到亚硒酸(H
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为___________。
(2)研究米乐M6 米乐平台表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应___________。
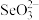
(4)关于硒单质及其化合物说法正确的是___________(填标号)。
(3)铝与氢氧化钠溶液反应的离子方程式________。您最近一年使用:0次2024/07/m6米乐官网 米乐M6平台入口0189 (0.65)【推荐3】W、X、Y、Z、Q、F是六种原子序数依次增大的前四周期元素,其中W的最外层电子数是其内层电子数的3倍,X是短周期中原子半径最大的元素,X、Y、Z为同周期元素,Y原子的核外电子总数是其最外层电子数的3倍,Z原子最外层有1个未成对电子,Q位于Y的不同周期,且它核外成单电子是同周期中最多的,F元素基态原子最外层有1个电子。请回答下列问题:
(1)W、X、Y、Z四种元素中第一电离能最小的是__________(填元素符号);Q原子的价电子排布式为________;
(3)W元素有两种同素异形体,W和X形成的化合物中含有非极性共价键的物质P,写出P与W的最简单氢化物反应的离子方程式__________________
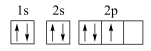
(4)下图是W元素的最外层电子排布图,它违背了电子排布的什么原则____________。
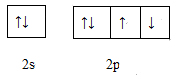
(5)Y单质和Z单质反应可生成原子个数比为1:5的化合物M和1:3的化合物N,与M中价态相同的Y的含氧酸根的立体构型为_____________。
(1)CO2的电子式是_____,包含的化学键类型为____(填“非极性”或“极性”)共价键。
(2)在温度高于31.26 ℃、压强高于7.39×106Pa时,CO2处于m6米乐官网 米乐M6平台入口超临界状态,称为超临界CO2流体,可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,超临界CO2萃取的优点有_________(答出一点即可)。

①写出次氟酸的结构并标出各元素的化合价__________________;
②次氟酸刹那间被热水分解得到既可表现氧化性(对NaI)又可表现还原性(对KMnO4)的溶液,写出次氟酸分解反应的化学方程式:____________________________。
(2) 氰(CN)2的化学性质与卤素(X2)很相似称为拟卤素,氰能和氢气反应生成HCN,其水溶液是一种酸。氰的氧化性比溴弱、比碘强。
(2)氢化钠与水反应的化学方程式为____________,反应的氧化剂为____________。该反应过程中,被破坏的化学键有____________(填数字序号,下同),形成的化学键有_______。
2022年诺贝尔化学奖授予在发展点击化学和生物正交化学方面贡献的三位科学家。点击化学的代表反应为Cu催化的叠氮-炔基Husigen环加成反应,
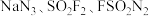
(2)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)

